近日,公共卫生学院卫生检验教研室在分析化学领域国际期刊《Analytical Chemistry》发表了题为“Ultrasensitive miRNA Detection Based on Magnetic Upconversion Nanoparticle Enhancement and CRISPR/Cas13a-Driven Signal Amplification”的研究论文,影响因子7.4。硕士研究生关丽雯为第一作者,郝先教授、未来技术学院王小磊教授为共同通讯作者。论文链接:https://pubs.acs.org/doi/10.1021/acs.analchem.3c03554
作为一种具有重要调节作用的小分子物质,miRNA常常作为众多早期疾病的生物标志物广泛应用于生物传感领域。因此开发具有高灵敏度和高特异度的miRNA检测平台至关重要。成簇规律间隔的短回文重复序列(CRISPR)/Cas13a 作为新型的具有高保真性和高效性的传感元件已被广泛运用于生物传感技术中,而UCNPs是一种具有众多优点的新型纳米发光材料。在这里,我们合成了一种磁性上转换纳米发光粒子(MUCNP),该粒子由Fe3O4@AuNPs和UCNPs经过双链DNA杂交偶联,在此基础上建立了基于CRISPR/Cas13驱动的信号放大和磁性上转换纳米粒子(CRISPR-MUCNP)平台用于灵敏检测miRNA。
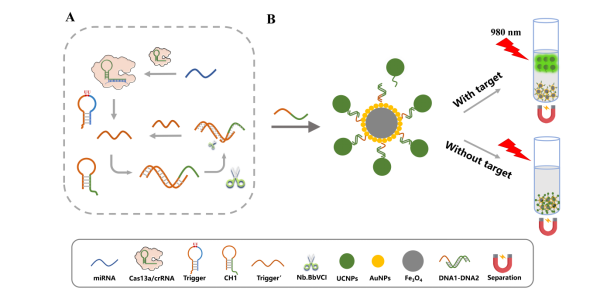
我们选择了血吸虫源sja-miR-2c5p作为本研究靶标进行实验。考虑到本研究所使用的LwaCas13a反式裂解活性更倾向于裂解核糖核苷酸尿嘧啶两侧的磷酸二酯键,我们设计了一种环部包含两个rU的触发器Trigger,当Cas13a被靶标激活后可以特异性地切割Trigger。紧接着Trigger’与CH1通过粘性末端打开发夹形成双链DNA。新形成的双链DNA被Nb.BbVCI在特定部位进行识别与切割。通过切割和链置换反应循环,可以产生大量的单链DNA产物。相对地,Cas13a 反式切割活性在靶标不存在的情况下被沉默,并且未切割的Trigger不能与CH1结合并触发下游反应。在这里,我们合成了一种磁性上转换纳米发光粒子(MUCNP),表面修饰了DNA1的Fe3O4@AuNPs和修饰了DNA2的UCNPs通过DNA杂交进行偶联从而形成MUCNP。单链DNA产物通过粘性末端将与DNA2相连接的UCNPs从MUCNP表面置换下来,随后利用磁铁分离除去剩余的MUCNP,这时上清液中只存在UCNPs。用980nm激光器照射上清液即可采集到稳定的发光信号。
综上所述,我们建立了一种具有高灵敏度和特异性的CRISPR-MUCNP检测平台。本平台结合了CRISPR/Cas13a的高保真度、酶循环扩增的信号放大性、光稳定性、UCNPs的低背景等优势,开发了一种高灵敏度、高特异性的miRNA检测方法,检测限低至83.2 fM。
本研究获得了国家自然科学基金(No.82160631、22277047和31860263),江西省重点青年项(20202ACB216002),江西双千计划(科技创新高水平人才项目,No.021021860218606),南昌大学医学院青年教师培养基金(No.PY201909)以及国家创新创业本科培养计划(No.202210403019)的支持。